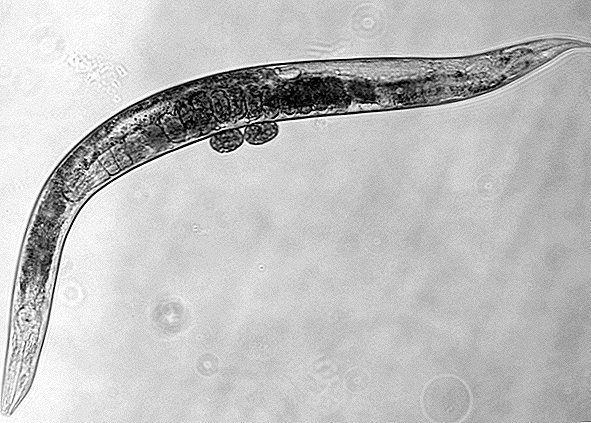
Bilim adamları, yuvarlak bir solucanın DNA'sındaki birkaç anahtar geni ayarlayarak, hayvanın ömrünü yaklaşık% 500 uzattı.
Hayatta büyük bir sıçrama: Ortalama bir yuvarlak kurt yaklaşık üç ila dört hafta yaşar. Ancak iki spesifik genin (DAF-2 ve RSKS-1) numaralandırılmaması durumunda, yaratıklar birkaç ay hayatta kalabilir.
Bilim adamları bu genleri uzun yıllar önce bağlamışlardı, bu genler kapatıldığında solucanların ve diğer canlıların yaşam süresinde bir artış olduğunu fark ettiler. Bununla birlikte, yaşlanma sürecinde genlerin kesin rolü bir sır olarak kaldı.
Şimdi, araştırmacılar bu iki gen ve mitokondri arasındaki noktaları birleştirdiler, bu da vücutta hücre fonksiyonunu besleyen küçük güç merkezleri. 2019'da Cell Press dergisinde yayınlanan bir araştırmaya göre, mitokondri bir organizma yaşlandıkça arızalanmaya başlıyor, ancak DAF-2 ve RSKS-1'in susturulması bu hasarı geciktiriyor ve ömrünü uzatıyor - en azından yuvarlak kurtlarda.
Yaşlanma karşıtı ilacın insanlar dahil memelilerde işe yarayıp yaramayacağını yalnızca zaman gösterecektir.
Domino etkisi
Bilim adamları ilk olarak DAF-2 ve yaşlanma arasındaki bağlantıyı 1990'ların başında, bir araştırma ekibi yuvarlak kurtların genin mutasyona uğramış bir versiyonunu taşıdıklarında normalden iki kat daha uzun yaşadıklarını keşfettiklerinde fark ettiler. Bulgu, genler ve onların yan ürünleri tarafından yönlendirilen yaşlanma çalışmasında yeni bir çağ başlattı.
Kaliforniya'daki Novato'daki Bucking Yaşlanma Araştırma Enstitüsü'nde profesör olan yazar Pankaj Kapahi, "Bu, sahadaki bir oyun değiştirici gibiydi ... çünkü insanlar tek bir genin ömrünü uzatabileceğine inanmaya başladı" dedi. .
Zamanla, araştırma grupları RSKS-1 de dahil olmak üzere daha uzun ömürlü genleri ortaya çıkardı, ancak kanıtlar bu genetik kod bölümlerinin tek başına çalışmadığını gösterdi. Bunun yerine, "sinyal yolları" olarak bilinen hücresel aktivitenin basamaklarını tetikleyerek, diğer genlerden oluşan bir ekip ve inşa etmeye yardımcı oldukları proteinlerle koordine ederler. Sinyal yollarını dominos sıraları olarak düşünün - bir domino devrildiğinde, diğerine düşer ve karmaşık bir zincir reaksiyonu başlatır.
DAF-2 ve RSKS-1'in her biri sırasıyla önemli bir sinyal yolunda bulunur: kan şekeri seviyelerini ve metabolizmasını kontrol etmeye yardımcı olan insülin sinyal yolu ve hücrelerin proteinleri nasıl ürettiklerini ve böylece nasıl büyüdüklerini ve çoğaldıklarını değiştiren TOR yolu. Ancak bu yolların yaşlanan bir organizmada nasıl kesiştiği bilinmiyordu, dedi Kapahi.
Bu yaşlanma karşıtı etkinin nereden geldiğini ortaya çıkarmak için Kapahi ve meslektaşları, her iki genin de kapatıldığı mutant yuvarlak solucanların hücrelerini gözetlediler. "Polimomal profil oluşturma" adı verilen bir teknik kullanarak ekip, hücrelerin herhangi bir anda hangi proteinleri inşa ettiğini izleyebilir. Protein yapımı sırasında, hücreler belirli bir proteinin üretimini arttırmak veya geri çevirmek için çeşitli mekanizmalar kullanabilir. Ekip, mutant solucanlarda hücrelerin normal solucanlara göre "sitokrom c" adı verilen bir proteinin daha az kopyasını yaptığını buldu.
İşte mitokondriler resme giriyor:
Sitokrom c mitokondrinin iç zarında görülür ve negatif yüklü elektronların yapısı içinden geçmesine yardımcı olur. Elektronların proteinden proteine bu transferi mitokondrilerin yakıt üretmesine izin verir - ancak mutant solucanlarda sitokrom c'nin olması gereken yerde bir boşluk ortaya çıkar. Yakıt normalde olduğu gibi verimli bir şekilde üretilemeyen mitokondri, enerji üretimini geri çevirir ve bunun yerine hasarlı dokuları onarmaya odaklanır.
Enerji depoları düşerken, AMPK adı verilen bir yakıt algılama enzimi yüksek vitese geçer ve solucanın daha verimli bir enerji metabolizması biçimine geçmesine yardımcı olur. Bu karmaşık olaylar zinciri, sonunda hücreleri sağlıklı ve yaşlılığa büyük ölçüde zararsız kalan uzun ömürlü bir yuvarlak kurt üretir.
"Proteinler yaşla birlikte hasar görürler ve bu yolların engellenmesiyle daha az hasar görürsünüz," dedi Kapahi. Buna ek olarak, araştırmalar, kaslar ve beyindeki gibi bazı dokuların, bu yollar boğulmuş olduğu sürece daha sağlıklı büyüyebileceğini ileri sürüyor.
Solucanlardan insanlara
Genel olarak, mutant solucanlar yaşlanma hücrelerini onarmak için hem protein hem de enerji üretimini geri çevirdi. Özellikle, hayvanların üreme hücrelerinde sitokrom c eksikliği bu sürecin anahtarı gibi görünüyordu. Onlar, solucanların düşük enerji modundayken üreme ile ilgili süreçleri beklemeye alabileceğini söyledi.
Kapahi, organizmalar açlık moduna itildiğinde benzer şekilde tepki veriyor - yeterli beslenme olmadan, hücresel sinyaller vücuda yavru üretmeye hazırlanmaktan "zaman aşımı" almasını söylüyor. Bu fikir 1990'larda eski yuvarlak kurtların çalışmasıyla da desteklenmektedir; Bu çalışmada, mutant solucanlar normal solucanlardan iki kat daha uzun yaşadı, ancak yaklaşık% 20 daha az yavru ürettiler.
Pasif bir süreç olmaktan çok, yuvarlak kurtta yaşlanma, metabolizmayı, protein yapısını ve potansiyel üremeyi düzenlemek için birlikte çalışan dağınık bir biyolojik yol karışıklığı içerir. Kapahi, insanlarda benzer yollar olmasına rağmen, bilim adamları yaşlanmanın her iki organizmada da aynı şekilde çalışıp çalışmadığını hala bilmiyorlar. Bir şey varsa, insanlarda yaşlanma daha karmaşık olabilir.
Harvard Tıp Fakültesi tıp profesörü ve Massachusetts Genel Hastanesi diyabet biriminin başkanı Dr. Joseph Avruch, e-postayla "Koruma, solucanlar ve memeliler arasındaki bu yollarda önemli ve önemli farklılıklar yok," dedi.
İnsülin ve TOR yollarındaki sinyalleri bozmak solucanların ömrünü uzatmış gibi görünse de, insanların aynı cevaba sahip olup olmayacağı belirsizdir.
Avruch, "Burada tanımlanan gen ağı… memelilerde benzer şekilde işlev görürse, farmakolojik müdahaleler mümkün olur." Dedi. Başka bir deyişle, ilk olarak solucanlarda yapılan yaşlanma karşıtı deneyler, herhangi birinin insanlarda çalışıp çalışamayacağını bilmeden önce memelilerde çoğaltılmalıdır.
Yaşlanma sürecine dahil olan patikalar “solucana çok özgü bir şey olabilir” dedi Kapahi. "Ama bu soruları sorup sormadığımızı asla bilemeyiz."












